
ㆍ2009년 기출
1. 다음 중 재결정 온도가 가장 낮은 금속은?
① Al
② Cu
③ Ni
④ Zn
해설 :
재결정온도란 냉간가공, 열간 가공 등에서 소성변형을 일으킨 결정이 가열되면 내부 응력이 서서히 감소하여 변형이 잔류하고 있는 원래의 결정입자에서 내부 변형이 없는 새로운 결정의 핵이 발생하고, 이것이 차츰 성장하여 원래의 결정 입자와 대치되어 가는 현상을 재결정이라고 하고, 이때 필요한 온도를 재결정 온도라고 한다.
※응력은 물체가 힘을 받는다면 그 힘을 내부에서 저항하는 힘을 말한다.
각 금속의 재결정 온도
철 500℃, 니켈 500~650℃, 텅스텐 1200℃, 백금 450℃, 금 200℃, 몰리브덴 900℃, 구리 200℃, 은 200℃
아연 15~50℃, 알루미늄 150℃, 마그네슘 150℃, 카드뮴 50℃, 주석 0℃
2. 실온까지 온도를 내려서 다른 형상으로 변형시켰다가 다시 온도를 상승시키면 어느 일정한 온도이상에서 다시 원래의 형상으로 변화하는 합금은?
① 제진합금
② 방진합금
③ 비정질합금
④ 형상기억합금
해설 :
제진합금은 감쇠능이 큰 합금을 말한다. ※감쇠능이란 물체가 진동을 흡수하는 성질이다.
방진합금은 구조 재료로 사용될 수 있는 강도와 인성을 지니고, 진동의 감쇠능이 커서 방진ㆍ방음의 구실을 하는 합금 비정질합금은 물질을 구성하는 원자나 이온이 주기성 배치를 하지 않은 비결정성 합금을 말한다.
형상기억합금이란 힘을 가해서 변형을 시켜도 본래의 형상을 기억하고 있어 조금만 가열해도 곧 본래의 형상으로 복원하는 합금이다.
형상 기억 효과를 나타내는 재료는 Ni, Ti, Cu, Zn, Al, Ag 등
형상 기억 합금 중 실용 합금 Ti-Ni, Cu-Au-Ni, Cu-Zn-Al 등이 있다.
참조 자료 <문제와 해설 403P. 형상기억합금>
3. 잔류 오스테나이트를 마텐자이트로 변화시키는 열처리 방법은?
① 연속냉각 변태 처리
② 등온 변태 처리
③ 항온 변태 처리
④ 심랭 처리
해설 :
심랭처리(서브제로 처리)는 담금질에 수반되는 잔류 오스테나이트의 변태를 촉진시키기 위한 냉각 조작이다.
강재의 담금질에 있어서 탄소, 니켈, 크롬, 망간 등의 함유량이 많을수록, 담금질 온도가 높을수록, 또한 담금질 가능한 한도내에서 냉각 속도가 작을수록 잔류 오스테나이트가 많다. 이것이 상온에서 서서히 분해하기 때문에 치수의 경년변화를와 담금질 경도의 불균일을 초래한다. 따라서, 냉동장치로 0℃이하로 냉각하여 마텐자이트 변태를 촉진시킨다.
냉각법은 드라이아이스 또는 액체 산소에의 침지, 암모니아 프레온의 단열 팽창을 이용하는 냉자고식 냉각 등이 있는데, 급격하게 냉각하는 것은 금물이다.
4. 지름이 10cm인 인장시험편을 시험하여 파단 후 지름이 8mm가 되었다면 단면 수축률은 몇 %인가?
① 20
② 36
③ 64
④ 80
해설 :
단면수축률 = {(원 단면적 – 파단후 단면적) / 원 단면적} * 100(%) ※단면적 = πR^2
=[(5*5*3.14) – (4*4*3.14)] / (5*5*3.14) * 100 = (78.5-50.24) / 78.5 * 100 = 36%
연신율 = {(늘어난길이 – 원래 길이) / 원래 길이} * 100 (%)
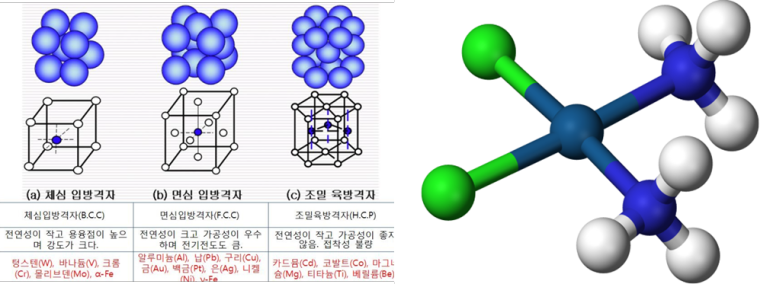
5. 면심입방격자의 배위수는 몇 개인가?
① 8
② 12
③ 16
④ 24
해설 :
배위수란 분자 및 결정에서 중심이 되는 원자 주위에 결합하고 있는 원자나 분자 또는 이온의 수를 말한다.
|
결정 구조
|
배위수
|
원자수
|
충진율 (%)
|
|
체심입방격자 (BCC)
Body centered cubic
|
8
|
2
|
68
|
|
면심입방격자 (FCC)
Face centered cubic
|
12
|
4
|
74
|
|
조밀육방격자 (HCP)
Hexagonal close packed
|
12
|
2
|
74
|
문제와해설 개정 9판 384P 참조

6. 피아노 선재, 레일 등을 제조할 때 사용되는 최경강으로 이 재료의 탄소함량으로 옳은 것은?
① 0.13~0.20%C
② 0.30~0.40%C
③ 0.50~0.70%C
④ 1.50~2.0%C
해설 :
최경강은 탄소 함유량이 0.5~0.6%이고 인장 강도가 70kg/㎟ 이상인 고탄소강, 강선 스프링 따위를 만드는데 쓴다.
7. 금속재료에 외부의 힘을 가하여 원하는 형태로 변형 시킴과 동시에 재료의 기계적 성질을 개선하는 가공법을 무엇이라 하는가?
① 용접
② 절삭가공
③ 소성가공
④ 분말 야금
해설 :
용접은 같은 종류 또는 다른 종류의 금속재료에 열과 압력을 가하여 고체 사이에 직접 결합이 되도록 접합 하는 방법 절삭가공은 성형하고자 하는 금속보다 경도가 큰 밀링머신, 선반 등 절삭 공구를 이용하여 금속으로부터 칩을 깎아내어 원하는 형상의 금속을 만드는 것을 말한다.
분말야금은 금속분말을 이용하여 마치 금속을 녹여 만든 것처럼 원하는 형태를 갖는 금속 물체를 만드는 것을 말한다.
8. 다음 중 저용융점 합금의 원소로 사용 되는 것이 아닌 것은?
① W
② Bi
③ Sn
④ In
해설 :
용융점은 물질이 고체에서 액체로 상태변화가 일어날 때의 온도이다. (=녹는점)
용융점이 가장 낮은 금속은 수은 (Hg) -38.4℃, 용융점이 가장 높은 금속은 텅스텐 (W) 3410℃ 이다.
저용융점 합금은 용융점이 231.9℃ 이하인 금속을 말한다. (Sn의 융점을 기준으로 한다.)
Bi 271.3℃, In 156.6℃
9. 다음 중 체심입방격자의 표시로 옳은 것은?
① LCC
② BCC
③ CPH
④ FCC
해설 :
배위수란 분자 및 결정에서 중심이 되는 원자 주위에 결합하고 있는 원자나 분자 또는 이온의 수를 말한다.
|
결정 구조
|
배위수
|
원자수
|
충진율 (%)
|
|
체심입방격자 (BCC)
Body centered cubic
|
8
|
2
|
68
|
|
면심입방격자 (FCC)
Face centered cubic
|
12
|
4
|
74
|
|
조밀육방격자 (HCP)
Hexagonal close packed
|
12
|
2
|
74
|
문제와해설 개정 9판 384P 참조
10. 냉간가공과 열간가공을 구별하는 기준이 되는 것은?
① 변태점
② 탄성한도
③ 재결정온도
④ 마무리온도
해설 :
재결정온도란 냉간가공, 열간 가공 등에서 소성변형을 일으킨 결정이 가열되면 내부 응력이 서서히 감소하여 변형이 잔류하고 있는 원래의 결정입자에서 내부 변형이 없는 새로운 결정의 핵이 발생하고, 이것이 차츰 성장하여 원래의 결정 입자와 대치되어 가는 현상을 재결정이라고 하고, 이때 필요한 온도를 재결정 온도라고 한다.
※응력은 물체가 힘을 받는다면 그 힘을 내부에서 저항하는 힘을 말한다.
철 500℃, 니켈 500~650℃, 텅스텐 1200℃, 백금 450℃, 금 200℃, 몰리브덴 900℃, 구리 200℃, 은 200℃
아연 15~50℃, 알루미늄 150℃, 마그네슘 150℃, 카드뮴 50℃, 주석 0℃
11. 청동의 기계적 성질 중 경도는 구리에 주석이 몇 % 함유 되었을 때 가장 높게 나타나는가?
① 10
② 20
③ 30
④ 50
해설 :
청동의 기계적 성질은
경도는 Sn 30%에서 최대가 되며, 25% 이상에서는 취성이 생긴다.
문제와해설 개정 9판 395P 참조
12. 다음 중 내열용 알루미늄 합금이 아닌 것은?
① Y-합금
② 코비탈륨
③ 로엑스(Lo-Ex)합금
④ 톰백
해설 :
톰백은 황금에 가장 가까운 빛깔을 지닌 구리합금으로 8~20%의 아연을 구리에 첨가하였다.
문제와해설 개정 9판 391P 참조
13. 다음 중 염화아연욕의 특징으로 옳은 것은?
① 주물 등에 직접 도금이 잘 된다.
② 도금액 중에서 수소취성이 많이 생긴다.
③ 액의 전도성이 낮아 욕전압이 높다.
④ 시안화합물을 사용하므로 시안 폐수가 생긴다.
해설 :
염화아연도금액의 장단점
-시안화물을 사용하지 않으므로 시안 폐수가 필요 없다.
-액의 전도성이 좋고, 광택 및 레벨링이 우수하다.
-수소취성이 거의 생기지 않는다.
-주물 등에 직접 도금이 가능하다.
-가스발생이 거의 없으므로 배기장치가 거의 필요 없다.
-작업중지 때도 양극판을 꺼내 놓을 필요가 없다.
-작업 범위가 좁다.
-균일 전착성이 나쁘다.
-부식성이 강해 설비의 관리가 필요하다.
문제와해설 개정 9판 153P 참조
14. 다음 중 알칼리탈지에 있어 금속을 부식시키는 pH 값이 가장 큰 것은?
① 아연
② 철강
③ 주석
④ 황동
해설 :
금속의 부식 범위(pH)
아연 10, 알루미늄 10, 주석 11, 황동 11.5, 철강 13
문제와해설 개정 9판 49P 참조
15. 황산구리 도금액에서 양극에 함인동판을 사용하는 이유로 가장 적절한 것은?
① 양극판의 소모가 적기 때문에
② 도금의 밀착성을 향상시키기 위하여
③ 도금액의 전기전도도를 향상시키기 위하여
④ 양극판에서 구리분말이 발생하는 현상을 줄이기 위하여
해설 :
양극판은 인을 함유한 (함인동판) 구리판을 사용하는 것이 균일하게 용해되고 슬러지 (sludge) 발생량도 적다.
문제와해설 개정 9판 145P 참조
16. 와트액을 분석한 결과 염화니켈의 농도가 부족하였을 때 취해야 할 조치로 가장 적절한 것은?
① 광택제를 보충한다.
② 양극전류밀도를 높인다.
③ 염산으로 pH를 조정한다.
④ 억제제(inhibitor)를 더 첨가한다.
해설 :
pH지, pH미터로 측정하여, pH가 높으면 구름이 끼기 쉽고 도금층이 취약하게 되기 쉬우므로 pH가 높으면 붕산, 황산, 염산 등으로 내리고, 낮을 때는 수산화나트륨, 수산화니켈, 탄산니켈 등으로 높여주어야 한다.
문제와해설 개정 9판 146P 참조
17. 다음 중 광택니켈도금에서 제1차 광택제의 주된 역할로 가장 적당한 것은?
① 피트를 방지한다.
② 광택을 향상시킨다.
③ 표면의 pH농도를 조절한다.
④ 내부 응력의 증가를 감소시킨다.
해설 :
광택니켈도금 와트액은 황산니켈, 염화니켈, 붕산의 세 가지 성분으로 이루어져 있다.
황산니켈은 니켈이온의 주공급원이며, 니켈이온의 농도가 높을수록 고전류 밀도로 작업이 가능하다.
염화니켈은 염소이온과 니켈이온을 공급하며 양극용해를 좋게 해주며, 전도성을 좋게하여 도금의 효율과 피복력을 좋게 하며, 과잉일 때는 내부응력을 증대 시킨다.
붕산은 pH 변화를 적게 해주는 완충제 역할을 해주며, 내부응력, 연성 등 물성도 개선 되며 도금 색상을 백색으로 내는데 중요한 역할을 한다.
광택제는 두 가지 이상의 유기광택제가 사용 되고 있는데,
1차 광택제는 내부응력을 적게 해주고 2차 광택제를 보조해주며,
2차 광택제는 도금면을 유리알 같이 좋은 광택을 만들어준다.
문제와해설 개정 9판 148P 참조
18. 다음 중 이온화 경향이 가장 큰 금속은?
① Ni
② Zn
③ Cu
④ Fe
해설 :
이온화경향이란 원자 또는 분자가 이온이 되려고 하는 경향을 말한다.
K > Ca > Na > Mg > Al > Zn > Cr > Fe > Cd > Co > Ni > Sn > Pb > (H) > Cu > Hg > Ag > Pt > Au
칼 카 나 마 / 알 아 크 철 / 카 코 니 / 주 납 / 수 구 / 수 은 백 금
이온화 경향이 큰 금속일수록 전자를 잃고 양이온이 되려는 경향이 있다. (반응성이 크다)
이온화 경향이 작은 금속일수록 쉽게 전자를 얻어 환원이 잘 된다. (반응성이 작다)
문제와해설 개정 9판 96P 참조
19. 강전해질 0.1M – HCl 과 0.01M – BaCl2 이 가지는 4개의 이온 농도가 틀리게 표현된 것은?
① HCl의 [H^+] = 0.1M
② HCl의 [Cl^-] = 0.1M
③ BaCl2 의 [Cl^-] = 0.01M
④ BaCl2 의 [Ba^2+] = 0.01M
해설 :
M 몰질량의 단위이다. 어떤 물질 1몰(mol)의 질량이다.
HCl은 강산으로 완전히 이온화 된다.
0.1M HCl의 경우 [H^+] = 0.1M이고 [Cl^] = 0.1M이다.
BaCl2는 강전해질로 완전히 이온화 된다. (이온 형태로 변화 된다. =물에 녹아 완전히 분리 된다.)
0.01M BaCl2의 경우, BaCl2는 Ba^2+와 2Cl^-로 이온화 된다.
[Ba^2+] = 0.01M
[Cl^-] = 2 x 0.01M = 0.02M이 된다.
20. 다음 중 용제탈지제가 갖추어야 하는 요건과 가장 거리가 먼 것은?
① 점도가 낮을 것
② 불연성이며, 인화성이 없을 것
③ 도금 재료를 침식, 부식시키지 않을 것
④ 유성에 대한 용해능력이 작을 것
해설 :
용제탈지의 용제 구비 조건
-유성에 대한 용해 능력이 클 것
-불연성이며 인화성이 없어야 한다.
-도금재료를 부식, 침식 시키지 말 것
-독성이 적고 냄새가 없어야 한다.
-안전하며 비점이 낮을 것
-증기 밀도 및 액상 비중이 클 것
-점도가 낮으며 표면장력이 작을 것
-회수가 쉬울 것
-유지비가 적고 가격이 저렴해야 한다.
문제와해설 개정 9판 48P 참조
21. 다음 중 전해연마의 특징으로 틀린 것은?
① 볼록한 부분이 쉽게 용해된다.
② 제품을 양극으로 하여 연마한다.
③ 표면적이 큰 물품도 균일하게 연마를 할 수 있다.
④ 음극은 납, 스테인리스 판, 탄소봉 등을 이용한다.
해설 :
전해연마는 고농도의 산이나 알칼리 용액에서 가공물을 양극으로 하여 전기적으로 용해시켜 표면을 평활하게 만드는 과정이다.
음극으로는 구리, 납, 스테인리스강 및 탄소봉 등이 사용된다. 양극인 금속의 표면에는 용해된 금속 이온이 전해질과 반응하여 전기저항이 큰 점액질과 전해 반응에 의해 생성된 산소가 혼재된 피막이 완만한 곡면의 형태로 뒤덮이게 된다.
돌출 부분의 저항이 오목한 부분에 비하여 적게 되어 돌출부에 전류가 집중되면서 우선 용해가 진행되어 전체적으로 평활한 표면이 얻어진다.
문제와해설 개정 9판 42P 참조
22. 다음 중 피로인산구리 도금액의 pH 범위로 가장 적절한 것은?
① 1 ~ 2
② 3 ~ 4
③ 5 ~ 6
④ 8 ~ 9
해설 :
피로인산구리는 P비로 관리를 한다. P비 = P2O7/Cu = P비를 7.0~8.0으로 관리한다.
문제와해설 개정 9판 145P 참조
23. 다음 중 핀홀(pin hole)에 대한 방지대책으로 적절하지 않은 것은?
① pH 값을 5.5 이상으로 조정한다.
② 약간 낮은 전류밀도로 작업한다.
③ 전처리 작업을 조건에 맞추어 철저히 한다.
④ 도금액의 교반을 좀 더 강하고 고르게 한다.
해설 :
도금액 중의 수소가스가 완전히 방출되지 못하며 도금면에 미세한 凸凹부분이 발생되는 것을 말한다.
특히 니켈도금에서 많이 볼 수 있는 현상이며 주 원인은 도금액 중의 유기불순물의 함유, pH의 불균일, 콜로이드 상태의 물질이 존재하는 것 등이다. 피트가 발생하면 미세한 凹이 생기기도 하는데 이와 같은 것을 핀홀이라고 하는데 도금층의 부식발생 원인이 된다.
문제와해설 개정 9판 36P 참조
24. 전기화학반응에 이용된 전기량과 전기량계로부터 구한 전체 통과전기량의 비를 무엇이라고 하는가?
① 전류밀도
② 전류효율
③ 분해전압
④ 전기화학당량비
해설 :
전류효율은 도금에 사용된 전기량의 몇 %가 실제적으로 도금에 소비 되었는가를 백분율로 나타낸 것을 말한다.
-음극전류효율(Effc)% = 도금량(g) / 이론석출량(g) * 100
-양극전류효율(Effa)% = 양극용해량(g) / 이론용해량(g) * 100
-양극, 음극 전류 효율 관계
Effc = Effa : 오랜 시간 도금을 해도 금속분의 변화가 없다.
Effc > Effa : 양극 용해량보다 도금량이 많으므로 액속의 금속분이 점차 희박해진다. (예, 니켈도금)
Effc < Effa : 음극석출량(도금량)이 양극 용해량보다 적으므로 액의 금속분이 점차 많아진다. (예, 알칼리 아연도금)
문제와해설 개정 9판 99P 참조
25. 다음 중 전처리 때 생긴 얇은 산화피막을 제거하여 표면을 활성 상태로 만들어 주는 역할을 하는 것은?
① 광택탈지
② 전해탈청
③ 알칼리탈청
④ 산담금
해설 :
도금할 소재 표면에 산화 피막을 최종적으로 제거함으로써 제품 표면을 활성화 상태로 만들어 주는 것으로 산 등이 들어 있는 수용액 중에 제품을 잠시 담그는 처리이다.
문제와해설 개정 9판 45P 참조
26. 도금 피막을 알아보는 시험방법으로 진한 염산에 침식 되어 녹색이 되었다면 이는 어떤 도금으로 되어 있는 것인가?
① 금도금
② 아연도금
③ 크롬도금
④ 니켈도금
해설 :
크롬도금의 특징
-외관이 보기 좋고 대기 중에서 변색이 없고, 염산 이외의 산에 대해서는 부식 되지 않는다.
-균열이나 핀홀이 생기기 쉽고 소재를 완전 피복하기가 어렵다.
-불용성 양극을 사용해야 한다.
-10배정도의 높은 전류밀도를 사용한다.
-음극전류효율이 15% 정도로 대단히 나쁘다.
-광택제 없이도 광택을 얻을 수 있다.
-액의 6가 크롬은 독성이 많아 공해 문제가 크다.
문제와해설 개정 9판 149P 참조
27. 다음 중 크롬도금액을 만들 때 무수크롬산과 촉매로 쓰이는 것은?
① 황산
② 붕산
③ 마그네슘
④ 니켈
해설 :
일반적인 크롬도금액은 무수크롬산과 황산을 중량비 100 : 1로 표준하여 작성한다.
문제와해설 개정 9판 149P 참조
28. 다음 중 전기도금시 걸이(rack)와 모선(bus bar)의 접촉 부분이 가장 잘 설계된 것은?
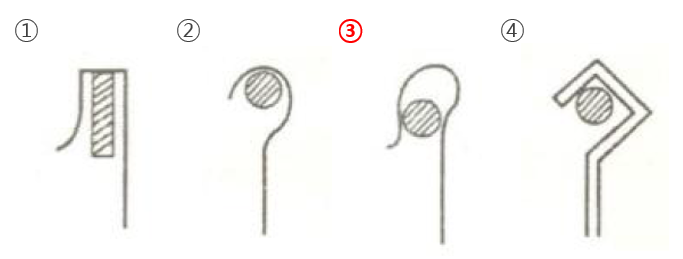
해설 :
걸이의 모형 좋음과 나쁨 이해하기
문제와해설 개정 9판 54P 참조
29. 도금한 제품에 페록실 시험(유공도시험)을 하는 것은 무엇을 측정하기 위한 것인가?
① 경도
② 내식성
③ 밀착성
④ 도금 두께
해설 :
내식성 시험의 종류는 유공도(페록실)시험, 염수분무시험(중성, 아세트산, CASS), 코로드코트시험, EC시험, 옥외방치시험, 아황산가스시험 등이 있다.
코로드코트시험은 부식액을 품고 있는 페이스트를 시험편에 도포 후 시간이 경과한 후 관찰하는 방법이다.
페록실시험 (페로시안칼륨, 페리시안칼륨, 염화나트륨, 염화암모늄, 암모니아수)
코로드코트시험 (질산구리, 염화제이철, 염화암모늄)
도금두께 시험 방법으로는 파괴식으로는 현미경 측정법, 분사시험법, 적하시험법, 전해시험법이 있고,
비파괴식으로는 맴돌이시험, 자기력식, 형광 X선, β선식, 중량차에 의한 방법 등이 있다.
문제와해설 개정 9판 308P 참조
30. 전기도금 중 알칼리 금 도금시 보급원으로 가장 적절한 것은?
① 시안화금칼륨
② 황산금
③ 염화금
④ 수산화금
해설 :
알칼리성(시안화) 금 도금액 조성 시안화금칼륨, 시안화칼륨, 탄산칼륨, 인산일수소칼륨이다.
중성 금도금액 조성은 시안화금칼륨, 인산이수소나트륨, 수산화칼륨, 시안화니켈칼륨이다.
산성 금도금액 조성은 시안화금칼륨, 인산이다.
문제와해설 개정 9판 157P 참조
31. 비중이 1.84인 황산(H2SO4) 11g을 부피로 환산하면 약 몇 mL가 되는가?
① 3
② 6
③ 9
④ 12
해설 :
체적 = 중량 / 비중
1.84 / 11 = 5.978
32. 시안화구리도금에서 도금액의 성분 중 다음 설명에 해당 하는 것은?
“도금액 중 최대 허용량은 60g/L 이며, 그 이상이 되면, 양극의 용해가 잘 되지 않고, 광택 및 평활성이
나빠져 조악한 석출면을 나타내게 된다.”
① 탄산나트륨
② 티오시안화칼륨
③ 시안화나트륨
④ 수산화나트륨
해설 :
탄산나트륨의 증가는 시안화나트륨과 수산화나트륨의 분해에 의한 것이다. 탄산 나트륨이 최대 허용값인 60g/L 근처에 도달하면 냉각법이나, 희석법, 석회법으로 제거한다.
문제와해설 개정 9판 143P 참조
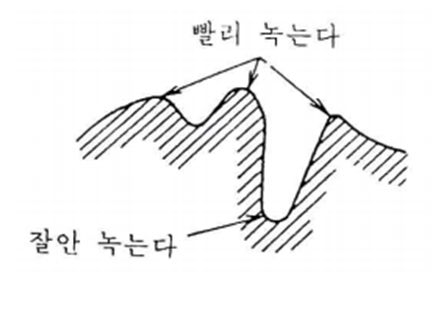
33. 다음 금속의 쌍을 황산에 담그거나 전지를 만들 때 외부 전류가 화살표 방향으로 흐르게 되는 것은?
① Zn → Ag
② Cu → Fe
③ Fe → Ag
④ Zn → Cu
해설 :
화학전지는 기본적으로 금속의 반응성 차이 (이온화 경향)에 의한 산화, 환원 반응으로 전기에너지가 생성 되는 원리이다.
※ 이온화경향은 용액속에서 원소가 이온이 되기 쉬움을 나타내는 것으로 금속의 종류마다 이온화 경향의 정도가 다르다.
이온화경향이란 원자 또는 분자가 이온이 되려고 하는 경향을 말한다.
K > Ca > Na > Mg > Al > Zn > Cr > Fe > Cd > Co > Ni > Sn > Pb > (H) > Cu > Hg > Ag > Pt > Au
칼 카 나 마 / 알 아 크 철 / 카 코 니 / 주 납 / 수 구 / 수 은 백 금
이온화 경향이 큰 금속일수록 전자를 잃고 양이온이 되려는 경향이 있다. (반응성이 크다)
이온화 경향이 작은 금속일수록 쉽게 전자를 얻어 환원이 잘 된다. (반응성이 작다)
문제와해설 개정 9판 96P 참조
34. 전해질이 음이온과 양이온으로 분리 되는 것을 무엇이라 하는가?
① 포화
② 전착
③ 전리
④ 확산
해설 :
이온은 전리로 인하여 생긴 입자(전기를 띄우고 있는)를 말한다.
전리는 수용액 중에서 이온으로 나누어지는 현상을 말한다.
전리도는 어떠한 물질이 수용액 속에서 전리 되는 정도가 다르게 되는데 이때 이온으로 전리 되는 비율을 말한다.
문제와해설 개정 9판 96P 참조
35. 10 x 10cm 의 판을 도금하는데 20A의 전류가 흐른다면 이 때의 전류밀도(A/dm²)는?
(단, 판의 두께는 무시한다.)
① 1
② 5
③ 10
④ 20
해설 :
전류밀도(A/dm²) = 전류의 세기(A) / 표면적(dm²)
전류(A) = 전류밀도(A/dm²) * 표면적(dm²)
표면적 = 10cm * 10cm * 2(양면) = 200㎠ = 2dm²
전류밀도 = 20A / 2dm² = 10A/dm²
문제와해설 개정 9판 312P 참조
36. 다음 중 페러데이의 법칙에 관한 설명으로 옳은 것은?
① 전극에 석출하는 물질의 양은 용액을 통과하는 전기량에 비례한다.
② 전극에 석출하는 물질의 양은 용액을 통과하는 전류에 반비례한다.
③ 전극에 석출하는 물질의 양은 용액을 통과하는 저항에 비례한다.
④ 전극에 석출하는 물질의 양은 용액을 통과하는 전압에 반비례한다.
해설 :
패러데이 법칙
-전해질 수용액 중에서 전극에 석출하는 물질의 양은 통과한 전기량에 비례한다.
-일정한 전기량에서는 전해질 수용액에서 전극에 석출하는 물질의 양은 이 물질의 화학당량에 비례한다.
문제와해설 개정 9판 98P 참조
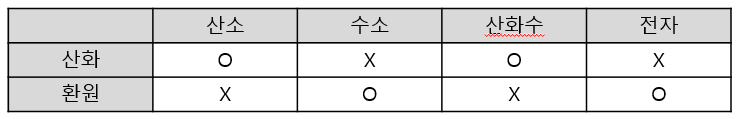
37. 다음 중 환원 반응을 나타내는 것은?
① 산소와 결합한다.
② 전자를 얻는다.
③ 수소를 잃는다.
④ 산화수가 증가한다.
해설 :
산화는 어떤 원자가 산소와 결합하거나, 수소화합물에서 수소를 일부 또는 전부를 잃거나, 어떤 원자가 전자를 얻는 변화, 어떤 원자의 산화수가 증가 되는 것을 말한다.
환원은 어떤 원자가 산소를 잃거나, 수소 화합물에서 수소와 결합하거나, 어떤 원자가 전자를 얻거나, 어떤 원자의 산화수가 감소 되는 것을 말한다.
문제와해설 개정 9판 97P 참조
38. 니켈도금의 경우 음극전류효율(Ec)과 양극전류효율(Ea)의 관계를 올바르게 나타낸 것은?
① Ec > Ea
② Ec < Ea
③ Ec = Ea
④ Ec < √Ea
해설 :
전류효율은 도금에 사용된 전기량의 몇 %가 실제적으로 도금에 소비 되었는가를 백분율로 나타낸 것을 말한다.
-음극전류효율(Effc)% = 도금량(g) / 이론석출량(g) * 100
-양극전류효율(Effa)% = 양극용해량(g) / 이론용해량(g) * 100
-양극, 음극 전류 효율 관계
Effc = Effa : 오랜 시간 도금을 해도 금속분의 변화가 없다.
Effc > Effa : 양극 용해량보다 도금량이 많으므로 액속의 금속분이 점차 희박해진다. (예, 니켈도금)
Effc < Effa : 음극석출량(도금량)이 양극 용해량보다 적으므로 액의 금속분이 점차 많아진다. (예, 알칼리 아연도금)
문제와해설 개정 9판 99P 참조
39. 다음 중 전해질의 전도도에 관한 설명으로 틀린 것은?
① 저항의 역수를 전도도라 한다.
② 용액은 전기전도에 대해서는 옴(Ohm)의 법칙이 적용 된다.
③ 전해질 용액에 전압을 가하면 이온이 이동하여 전류가 흐른다.
④ 전류의 양은 전해질의 저항에 비례하므로 저항이 작을수록 전도성은 좋다.
해설 :
저항은 전류를 통하는 것의 길이, 굵기, 온도에 따라 그 수치가 변하기 때문에 전선이 굵어질수록 같은 길이의 것이라면 저항은 감소되고 전선의 길이가 길어질수록 같은 굵기라면 저항은 증가된다. 온도가 상승되면 저항도 증가되는 금속이 있고, 온도가 상승하면 저항이 감소되는 것은 전해질 용액이다.
전류의 양은 전해질의 저항에 반비례한다. 즉, 저항이 작을수록 전류가 더 많이 흐르므로 전도성이 좋다고 할 수 있다.
참조 자료 <문제와 해설 53P. 저항의 변화>
40. 아연이 산성 용액에서 용해되는 반응 중 음극에서 일어나는 반응으로 옳은 것은?
① 2H^+ + 2e^- → H2
② Zn → Zn^2+ + 2e^-
③ O2 + 4H^+ + 4e^- → 2H2O
④ 2OH^- + 2e^- → H2O + ½ O2
해설 :
황산구리도금의 음극 반응
Cu^2+ + 2e (전자) → Cu
2H2 + 2e (전자) → H2 (수소 가스 발생)
황산구리도금의 양극 반응
Cu → Cu^2+ + 2e
H2O → 2H^+ + 1/2O2 +2e (산소가스 발생)
문제와해설 개정 9판 144P 참조
41. 알루미늄 합금을 알칼리계의 처리액에 전처리할 경우 합금 성분에 의해 스머트가 발생하는데 이러한 스머트의 제거 방법으로 가장 적절한 것은?
① HNO3에 침지한다.
② H3PO4에 침지한다.
③ HCl에 침지한다.
④ NaOH에 침지한다.
해설 :
산처리 및 알칼리 처리 후 표면에 남아 있는 검은 물질(피막)로서 스머트라고 하는데 존재 시에는 밀착 불량을 일으킨다.
질산은 산화성 산으로 비산화성 산에 비해서 스머트 제거에 효과적이다.
문제와해설 개정 9판 44P 참조
42. 화학 니켈 도금액에서 황산니켈의 조성은 20g/L가 적당하다고 한다. 50L의 도금조에 80%가 되도록 도금액을 만들고자 할 때 필요한 황산니켈의 양은 몇 g 인가?
① 400
② 600
③ 800
④ 1000
해설 :
전체 용량 = 20g/L * 50L = 1000g/L
1000 * 0.8 (80%) = 800g
43. 유해 환경에서 사용하는 방독마스크는 산소농도가 몇 % 이상인 장소에 착용하여야 하는가?
① 15%
② 16%
③ 18%
④ 20%
해설 :
방독마스크는 산소 농도가 18% 이상인 장소에서 사용하여야 하고, 고농도와 중농도에서 사용하는 방독 마스크는 전면형(격리식, 직결식)을 사용해야 한다.
44. 다음 중 경도에 따른 양극산화피막의 분류에 있어 경질 피막에 해당하는 것은?
① 비커스 경도(HV) 350 ~ 450
② 비커스 경도(HV) 250 ~ 350
③ 비커스 경도(HV) 150 ~ 250
④ 비커스 경도(HV) 150 이하
해설 :
전해온도를 저온 10 ~ -10℃에서 작업하며, 피막의 두께가 20㎛ 이상일 때 경질피막이라 한다.
초경질피막 (Hv) 450이상, 경질피막 350~450, 반경질피막 250~350, 보통피막 150~250, 연질피막 150 이하
문제와해설 개정 9판 227P 참조
45. 다음 중 양극산화법에서 많이 사용 되는 알루미늄의 재료로 가장 적절한 것은?
① 압연괴로 50.0%의 알루미늄
② 압연관재로 75.9%의 알루미늄
③ 압연봉재로 85.0%의 알루미늄
④ 압연판재로 99.8%의 고순도 알루미늄
해설 :
알루미늄의 재료로는 고순도의 알루미늄이 적합하다.
문제와해설 개정 9판 223P 참조
46. 다음 중 크롬 폐수 처리에서 3가 크롬의 침전반응에 사용 되는 약품은?
① MgO3
② NaOCl
③ NaOH
④ H2SO4
해설 :
6가 크롬은 3가로 환원 시킨 후 →
3가 크롬의 침전 반응 : Cr2(SO4)3 + 6NaOH → 2Cr(OH)3 + 3Na2SO4
Cr2(SO4)3(황산크롬), 6NaOH(수산화나트륨), 2Cr(OH)3(수산화크롬), 3Na2SO4(황산나트륨)
문제와해설 개정 9판 312P 참조
47. 다음 중 금속용사법의 장점으로 틀린 것은?
① 윤활성이 좋고 내마멸성이 크다.
② 금속 이외의 합금, 비금속 물질에도 가능하다.
③ 피막의 형성 속도가 빠르고 두꺼운 막을 형성할 수 있다.
④ 다른 표면 처리법보다 내식성이 우수하며, 분진의 발생이 적다.
해설 :
금속용사법의 장점
-금속용사는 그 가공물의 크기에 관계 없이 할 수가 있으므로 두께는 용사횟수를 거듭하면 얼마든지 두껍게 할 수 있다.
-소재가 유리, 목재, 종이, 콘크리트, 알루미늄, 스테인리스강 등 어떠한 제품도 단시간에 두꺼운 도금을 할 수가 있다.
-다공성의 피막이며 산화물을 품고 있으므로 윤활유 침투가 잘되어 내마모성이 크다.
-장치가 소형이고, 설비비가 적게 들며, 단시간에 숙련이 된다.
금속용사법의 단점
-소재와 결합이 기계적이고 용사입자가 용착 되어 있지 않아 떨어지기 쉽다.
-피막층은 방식 효과가 국한 되어 있고, 기계적 화학적으로 약하다.
-전처리에 비산금속을 사용하므로 비위생적이다.
-용사시 소모 되는 양이 많다.
용사방법의 전처리 방법으로는 샌드블라스트, 쇼트블라스트, 조각법(스크래퍼를 이용하여 표면을 긁어 내는 방법), 용착법(소지를 열과 압력을 가하여 용융시켜 금속을 적층 시켜 결합하는 방법), 몰리브덴 합금 용사법이 있다.
문제와해설 개정 9판 231P 참조
48. 버프 연마제 중 산화크롬이 주원료이며, 광택연마제로 가장 많이 사용되는 것은?
① 크로커스
② 백봉
③ 적봉
④ 청봉
해설 :
트리폴리(Tripoli) : 중연마용으로 무수규산 규석분이 주성분 (SiO2)
크로커스(Crocus) : 산화철 (Fe2O3)의 미분말 혼합
비엔나라임(Vienna lime) : 광택 연마용 (MgO, CaO)
백봉 : 비금속용 (Al2O3)
청봉(Green rouge) : 광택 연마용, 산화크롬 (Cr2O3)이 주원료
적봉(Rouge) : 금, 은 광택연마 (Fe2O3)
흑봉 : 고무, 플라스틱 연마용
문제와해설 개정 9판 39P 참조
49. 냉간압연강대의 연속도금법이며 용융도금의 문제점인 산세와 플러스 작업을 행하지 않는 용융도금방법은?
① 센지미어
② 차콜와이프법
③ 갈바닐링법
④ 스팽글법
해설 :
용융주석도금 중 납에 15~20%의 주석을 첨가해 도금한 강판을 턴 도금판이라 부른다.
용융아연도금 중 강판의 연속도금을 센지미어법(Sendzimer)이라고 하고, 강선의 도금을 패턴팅 (Patentin)이라고 한다.
문제와해설 개정 9판 229P 참조
50. 다음 중 약품에 의한 사고 발생시 응급처치로 적절하지 않은 것은?
① 수산화칼슘을 마셨을 때에는 물을 많이 마신다.
② 황산구리가 피부에 묻었을 때에는 물로 충분히 씻는다.
③ 암모니아를 마셨을 때에는 레몬 주스나 우유 등을 마신다.
④ 수산화나트륨이 피부에 묻었을 때에는 탄산수소나트륨 용액으로 씻어 낸다.
해설 :
각종 약품 취급방법 및 응급 조치법
문제와해설 개정 9판 338P 참조
51. 다음 중 버프연마에 있어 목적하는 평활도에 따라 공정을 3단계로 구분할 때 올바른 것은?
① 거친연마 → 중간연마 → 광택연마
② 자유연마 → 배럴연마 → 표면연마
③ 미세연마 → 조도연마 → 전해연마
④ 전해연마 → 배럴연마 → 광택연마
해설 :
평활도에 따른 연마 방법은 거친연마 → 중간연마 → 광택연마 순이다.
문제와해설 개정 9판 39P 참조
52. 다음 중 화성처리에 관한 설명으로 옳은 것은?
① 화성처리는 양극 산화처리 방법의 일종이다.
② 화학적으로 금속 표면에 방식 피막을 형성하는 것이다.
③ 도료 도장으로 금속표면에 방식보호와 취성을 주는 것이다.
④ 화성처리는 물리ㆍ기계적으로 금속 내부에 피막을 형성 하는 것이다.
해설 :
화성처리는 크로메이트처리와 인산염 피막처리를 말한다.
문제와해설 개정 9판 213P 참조
53. 무전해 구리 도금액의 조성 중 성분과 그 역할이 잘못 연결된 것은?
① 롯셀염 : 촉진제
② 포르말린 : 환원제
③ 탄산나트륨 : pH완충제
④ 수산화나트륨 : pH조정제
해설 :
무전해 구리도금의 원리는 구리이온에서 환원제에 의해 금속구리를 석출시키며, 전도성 부여를 목적으로 행한다.
구리이온의 공급(황산구리), 환원제(포르말린), 포환
착화제(롯셀염,EDTA), pH조정제(수산화나트륨), 롯착 수정
pH완충제(탄산나트륨), 안정제(티오요소, 시안화나트륨 등), 습윤제(계면활성제) 탄충 티안
문제와해설 개정 9판 220P 참조
54. 다음 중 플라스틱상의 도금에서 표면 감수성 처리와 가장 관계가 깊은 것은?
① NaHSO3
② BaCl2
③ SnCl2
④ K2CrO4
해설 :
엑셀러레이션은 캐탈리스팅 후 주석, 팔라듐 콜로이드가 플라스틱 표면에 흡착 되며 금속 팔라듐 핵이 표면에 남게 된다. 표면에 존재하는 과잉의 주석 산화물을 제거하여 금속 팔라듐을 노출 시켜 주는 작업이다.
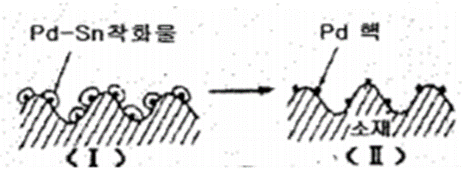
문제와해설 개정 9판 219P 참조
55. 다음 중 금속 용사법에서 용사층의 밀착성을 좋게 하기 위한 전처리법으로 적당하지 않은 것은?
① 조각법
② 광택연마법
③ 숏블라스트
④ 샌드블라스트
해설 :
금속용사법의 장점
-금속용사는 그 가공물의 크기에 관계 없이 할 수가 있으므로 두께는 용사횟수를 거듭하면 얼마든지 두껍게 할 수 있다.
-소재가 유리, 목재, 종이, 콘크리트, 알루미늄, 스테인리스강 등 어떠한 제품도 단시간에 두꺼운 도금을 할 수가 있다.
-다공성의 피막이며 산화물을 품고 있으므로 윤활유 침투가 잘되어 내마모성이 크다.
-장치가 소형이고, 설비비가 적게 들며, 단시간에 숙련이 된다.
금속용사법의 단점
-소재와 결합이 기계적이고 용사입자가 용착 되어 있지 않아 떨어지기 쉽다.
-피막층은 방식 효과가 국한 되어 있고, 기계적 화학적으로 약하다.
-전처리에 비산금속을 사용하므로 비위생적이다.
-용사시 소모 되는 양이 많다.
용사방법의 전처리 방법으로는 샌드블라스트, 쇼트블라스트, 조각법(스크래퍼를 이용하여 표면을 긁어 내는 방법), 용착법(소지를 열과 압력을 가하여 용융시켜 금속을 적층 시켜 결합하는 방법), 몰리브덴 합금 용사법이 있다.
문제와해설 개정 9판 231P 참조
56. 다음 중 금속 용사법에서 용사막에 대한 설명으로 틀린 것은?
① 산화물이 함유된다.
② 다수의 기공이 존재한다.
③ 인장강도와 내굴곡성이 크다.
④ 소재와 피막의 밀착은 기계적으로 이루어진다.
해설 :
55번 설명과 동일
문제와해설 개정 9판 231P 참조
57. 아연계 인산염 피막처리액의 액관리에 유용한 산비를 구하는 식으로 옳은 것은?
① 전산도 x 유리산도
② 전산도 / 유리산도
③ 전산도 + 유리산도
④ 전산도 - 유리산도
해설 :
전산도를 유리 산도로 나눈 값을 산의 비라고 한다. (전유)
각 처리 액을 통해서 이 산의 비가 가장 중요한 의미를 가지게 된다.
문제와해설 개정 9판 213P 참조
58. 다음 중 피막이 지니는 자기적 성질을 이용하기 위한 목적으로 실시 되는 것은?
① 무전해 구리 도금
② 무전해 금 도금
③ 무전해 수은 도금
④ 무전해 코발트 도금
해설 :
강자성체는 외부에서 자기장을 걸어주었을 때 그 자기장의 방향으로 강하게 자화된 뒤 외부 자기장이 사라져도 자화가 남아 있는 물질을 말한다. Fe, Ni, Co (강철니코)
상자성체는 외부의 자기장이 있으면 자기적 성질을 가지지만, 외부의 자기장이 사라지면 다시 자기적 성질을 잃는 성질이다. Al, Pt, Sn, Mn, Cr (상알백주망크)
반자성체는 외부 자기장에 반대 반향으로 자기모멘트를 가지는 물질을 말한다.
Cu, Sb, Zn, Ag, Au, Bi (반구안아은금비)
문제와해설 개정 9판 383P 참조
59. 면적 1dm^2의 양극 알루미늄에 1A/min의 전기량을 통과 시킬 때 생성 되는 피막의 중량은 약 몇 mg인가?
(단, 알루미늄과 산소의 원자량은 각각 27, 16이며, Faraday 상수는 96500, 전류 효율은 100%이다.)
① 5.29
② 10.57
③ 15.86
④ 21.14
해설 :
양극 산화의 알루미늄 피막은 Al2O3가 생성된다.
2Al + 3O3 = Al2O3 2*3가 = 6F
27 * 2 + 16 * 3 = 102
즉 6Faraday에 대해 Al2O3가 102g 생성하므로 60초간에는
(102*60) / (6*96500) = 0.0105699g = 10.57mg
문제와해설 개정 9판 98P 참조
60. 다음 중 금속 표면에 알루미늄을 침투시키는 방법은?
① 크로마이징
② 칼로라이징
③ 세라다이징
④ 실리코나이징
해설 :
금속침투법의 종류로는
세라다이징(아연), 크로마이징(크롬), 칼로라이징(알루미늄), 실리코나이징(규소), 보로나이징(붕소) 가 있다.
문제와해설 개정 9판 233P 참조
'ㆍ공부 자료 > ㆍ기능사' 카테고리의 다른 글
| 5. 표면처리기능사 문제 풀이 (2010년) (7) | 2024.09.07 |
|---|---|
| 4. 표면처리기능사 문제 풀이 (2011년) (3) | 2024.09.07 |
| 3. 표면처리기능사 문제 풀이 (2012년) (1) | 2024.09.07 |
| 3. 표면처리기능사 문제 풀이 (2013년) (4) | 2024.09.06 |
| 2. 표면처리기능사 문제 풀이 (2014년) (6) | 2024.09.06 |



