
ㆍ표면처리 기술사 제135회 1교시
8. 전해질 수용액 반응식 aA+bB→cC+dD에서 평형상수[K] 값을 설명하시오.
1. 전해질 수용액에서의 화학 평형상수(K)는 반응물과 생성물의 농도 또는 활동도 비율을 정량적으로 나타내는 값으로, 다음과 같은 기본 원리로 설명 된다.
ㆍ평형상수의 K의 정의
균형 맞춘 화학 반응식 aA + bB ⇌ cC + dD에서 평형상수(K)는 다음과 같이 표현 된다.
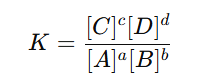
[A],[B],[C],[D] : 각 물질의 평형 상태에서의 몰 농도 (mol/L)
a, b, c, d: 화학 반응식의 계수
K : 온도에 따라 일정한 값 (같은 반응일 경우)
예시)
다음 반응의 평형상수를 구하시오:
Fe3+ + SCN- = FeSCN2+
어느 수용액에서 평형에 도달했을 때의 이온 농도가 다음과 같다고 가정한다.
[Fe3+]=1.0×10−4mol/L
[SCN−]=2.0×10−4mol/L
[FeSCN2+]=1.5×10−4mol/L
평행상수 K 계산 :
K = (FeSCN2+) / [(Fe3+)(SCN-)]
K = (1.5 * 10-4) / [(1.0 * 10-4)(2.0 * 10-4)
= (1.5 * 10-4) / [(2.0 * 10-8)
= 7.5 * 103
2. 전해질 반응의 특성
ㆍ이온화와 활동도
-전해질은 수용액에서 이온으로 해리되며, 이때 실제 농도 대신 활동도(activity)를 사용하여 비이상적 행동을 보정 한다.
활동도는 a=γ⋅c로 표현되며 (γ: 활동도계수), 이온 세기가 높을수록 γ는 감소 한다.
ㆍ이온 세기의 영향
첨가된 전해질은 반응의 이온 세기를 증가시켜 평형상수(K')를 한계값(K)과 다르게 만든다. 이 효과는 반응에 참여하는 이온의 전하량에 따라 크게 달라진다.
ㆍ평형상수의 종류
농도 평형상수(Kc): 몰농도 기반
압력 평형상수(Kp): 기체 반응에서 부분압 사용
용해도곱(Ksp): 포화용액에서의 이온 농도 곱
3. 반응지수(Q)와의 관계
반응지수(Q)는 평형이 아닌 상태에서의 농도 비율로, Q<K일 경우 정반응이 진행되어 평형에 도달한다.
4. 온도의 영향
평형상수는 온도에만 의존하며, 농도나 압력 변화에는 영향을 받지 않는다.
5. 요약
전해질 수용액의 평형상수는 반응 종의 농도 또는 활동도, 화학식 계수, 온도를 종합적으로 고려하여 결정된다.



